인공지능(AI)을 활용해 항암제의 효과를 저하하는 ‘세포 간 이질성’의 원인을 밝혀내고, 이를 극복할 수 있는 전략을 제시한 연구 결과가 발표됐다.
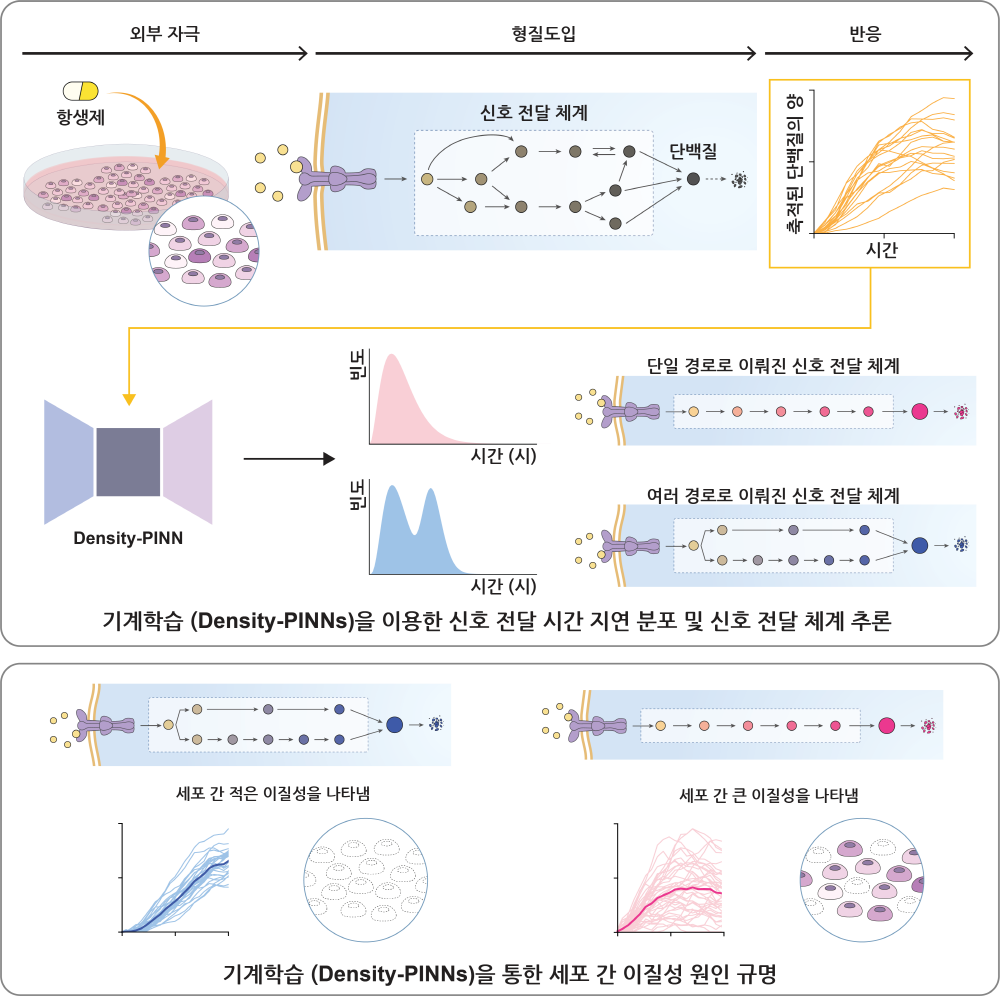
- 세포가 항생제 스트레스에 노출되면, 신호 전달 경로를 통해 반응 단백질이 생산된다. Density-PINNs는 축적된 반응 단백질의 시계열 자료를 이용하여 신호 전달 시간 지연 분포를 추론하며, 이 분포의 모양은 신호 전달 체계의 구조에 대한 정보를 준다(위).
- 이를 통해 병렬 구조를 갖는 세포 신호 전달 체계가 항생제에 대한 반응의 세포 간 이질성을 크게 감소시킨다는 사실을 규명했다(아래).
항암 효과 낮추는‘세포 간 이질성’극복 전략 찾았다
기초과학연구원(IBS) 수리 및 계산과학 연구단 의생명 수학 그룹 김재경 CI(Chief Investigator, KAIST 수리과학과 교수) 연구팀은 AI를 이용해 동일 외부 자극에 개별 세포마다 반응하는 정도가 다른 ‘세포 간 이질성’의 근본적인 원인을 찾아내고, 이질성을 최소화할 수 있는 전략을 제시했다.
연구팀은 세포가 외부 자극에 반응하는 신호 전달 체계(signaling pathway)가 세포 간 이질성에 영향을 미친다는 점에 착안했다. 신호 전달 체계는 세포가 외부 환경과 상호작용하며 생존하는 데 핵심적인 역할을 한다.
Density-PINNs를 통한 세포 간 이질성의 해석
연구팀은 기계 학습 방법론인 ‘Density-PINNs(Density Physics-Informed Neural Networks)’를 개발해 신호 전달 체계와 세포 간 이질성의 연결고리를 찾았다. Density-PINNs는 시간에 따라 축적된 반응 단백질의 양을 이용해 신호 전달 소요 시간의 분포를 추론할 수 있다. 이 분포는 신호 전달 체계가 몇 개의 경로로 구성됐는지를 알려준다.
연구팀은 실제 대장균의 항생제에 대한 반응 실험 데이터에 Density-PINNs를 적용하여 세포 간 이질성의 원인도 찾았다. 신호 전달 체계가 단일 경로로 이뤄진 때(직렬)에 비해 여러 경로로 이뤄졌을 때(병렬)가 세포 간 이질성이 적다는 것을 알아냈다.
연구팀은 “신호 전달 체계가 병렬 구조일 경우 극단적인 신호가 서로 상쇄되어 세포 간 이질성이 적어지는 것으로 보인다”며 “신호 전달 체계가 병렬 구조를 보이도록 약물이나 화학 요법 치료 전략을 세우면 치료 효과를 높일 수 있을 것으로 기대된다”고 말했다.
연구 결과는 2023년 12월 26일 국제학술지 셀(Cell)의 자매지인 ‘패턴스(Patterns)’에 실렸으며, 현장에서의 응용 가능성에 대한 기대가 높아지고 있다.
※ 논문명: Density physics-informed neural networks reveal sources of cell heterogeneity in signal transduction
출처 : 기초과학연구원
뇌과학이 제시하는 AI 혁명, NMDA 수용체가 열어가는 미래
뇌과학과 AI의 융합, NMDA 수용체 모델이 인공지능의 기억 통합 능력을 혁신적으로 향상시키고 있습니다. NeurIPS에서 인정받은 이 연구는 미래 인공지능의 새로운 시대를 열어갑니다. 뇌과학이 제
webdraw.tistory.com
'의학' 카테고리의 다른 글
| 이제는 무선으로, ‘나노-자기유전학’ 기반 파킨슨병 치료법 개발 (0) | 2024.02.04 |
|---|---|
| 오미크론 돌파감염, 미래 변이에도 면역력 강화 (0) | 2024.01.29 |
| 뇌 속 노폐물을 청소하는 허브 찾았다! 치매 예방의 열쇠 (0) | 2024.01.15 |
| 비자나무 잎 정유, 천식 치료의 새로운 희망 (0) | 2023.11.21 |
| 대사이상 지방간 환자, 알코올 섭취 시 심혈관질환 위험 2배↑ (0) | 2023.11.19 |









